2020. december 1-jén sikeresen elindult az EUDAMED adatbázis 1. modulja, az Actors modul. Ebben a modulban valósul meg a jövőben a gazdasági szereplők regisztrációja és nyilvántartása.
Az orvostechnikai eszközök európai szabályozását előíró MDR Rendelet alkalmazásba vételéig kevesebb már kevesebb mint 6 hónap áll rendelkezésére az érintett vállalkozásoknak.
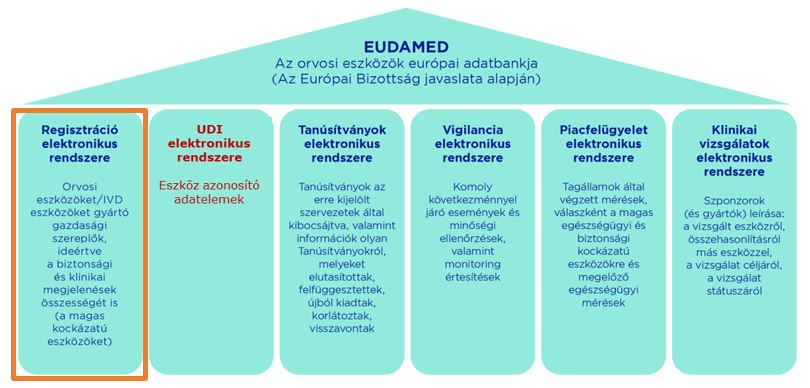
Az MDR Rendelet fontos eleme az a központi EU adatbázis, amely 6 modulból áll.
2020. december 1-jén sikeresen elindult az EUDAMED adatbázis 1. modulja, az Actors modul. Ebben a modulban valósul meg a jövőben a gazdasági szereplők regisztrációja és nyilvántartása.
Az Actors modul publikusan is elérhető és lehetőség nyílik a nyilvántartott szereplőkre történő keresés.
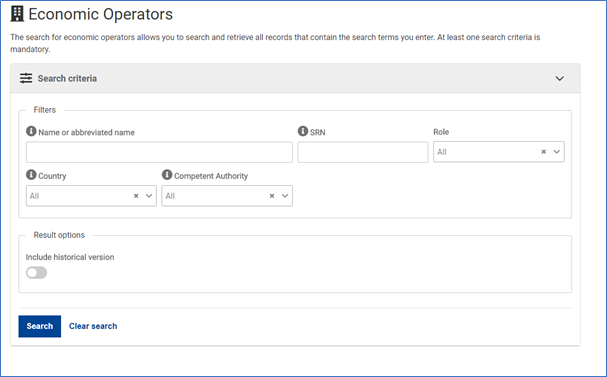
Várhatóan 2021. Q1-ben nyitják meg a következő két modult, az UDI és a Tanúsítványok modult. Ezen modulok szükségesek az orvostechnikai eszközök EUDAMED-be történő regisztrációjához. Az UDI modulban történik az eszköz regisztrációja a gyártó által, míg a hozzá kapcsolódó tanúsítványokat a Tanúsítvány modulban a Kijelölt szervezetek (Notified Body) töltik fel.
Önök már felkészültek 2021. május 26-ára?
Tájékozódjon: https://gs1hu.org/iparagi-megoldasok/egeszsegugy/orvostechnikai-eszkozok
Kérdés esetén keresse kollégáinkat: udi@gs1hu.org
AZ EUDAMED alkalmazásba vételéről várhatóan az OGYÉI ad hamarosan tájékoztatást, ezért javasoljuk az OGYÉI hírlevelére történő feliratkozást, illetve a korábbi hírlevelek áttanulmányozását: https://www.ogyei.gov.hu/?url=hirlevel_feliratkozas
https://www.ogyei.gov.hu/mdr_hirlevel_archivum
Forrás: https://ec.europa.eu/health/md_eudamed/actors_registration_en