 Az európai gyógyszerhamisítás elleni irányelvet (FMD, Falsified Medicines Directive - 2011/62/EU irányelv) kiegészítő, az emberi felhasználásra szánt gyógyszerek külső csomagolásán elhelyezendő biztonsági elemekre vonatkozó (EU 2016/161) rendelet könnyebb értelmezése és az előírások betartása érdekében az Európai Unió Bizottsága rendszeresen közzéteszi a leggyakrabban felmerülő kérdésekre adott hivatalos válaszait.
Az európai gyógyszerhamisítás elleni irányelvet (FMD, Falsified Medicines Directive - 2011/62/EU irányelv) kiegészítő, az emberi felhasználásra szánt gyógyszerek külső csomagolásán elhelyezendő biztonsági elemekre vonatkozó (EU 2016/161) rendelet könnyebb értelmezése és az előírások betartása érdekében az Európai Unió Bizottsága rendszeresen közzéteszi a leggyakrabban felmerülő kérdésekre adott hivatalos válaszait.
A legújabb „Kérdések – Válaszok” dokumentumot, amely immár a 16. verzió, szeptember végén publikálta az EU Bizottság. Az előző verzióhoz képest a következő módosítások találhatók a dokumentumban.
 Számos patikában okozott gondot, hogy a szkennerek nem megfelelően olvasták a gyógyszereken található kódot vagy a patikusok nem tudták a szemmel olvasható információkból egyértelműen értelmezni, hogy milyen karaktereket tartalmaz a kód (pl: O vagy nulla, 1 vagy nagy I, stb.). Ezért az EU Bizottsága ajánlást fogalmazott meg arra vonatkozóan, hogy milyen karaktereket nem javasolnak feltüntetni a sorozatszámban és a gyártási tételszámban (2.23 kérdés).
Számos patikában okozott gondot, hogy a szkennerek nem megfelelően olvasták a gyógyszereken található kódot vagy a patikusok nem tudták a szemmel olvasható információkból egyértelműen értelmezni, hogy milyen karaktereket tartalmaz a kód (pl: O vagy nulla, 1 vagy nagy I, stb.). Ezért az EU Bizottsága ajánlást fogalmazott meg arra vonatkozóan, hogy milyen karaktereket nem javasolnak feltüntetni a sorozatszámban és a gyártási tételszámban (2.23 kérdés).
Pontosították, hogy milyen esetekben szükséges kivizsgálni az egyes incidenseket (7.20 kérdés), mivel a sok különböző hibaüzenet alapján a patikusok sok esetben nem tudják, hogy mikor kell jelenteni a hibát, és mely esetekben adható még ki az adott gyógyszer a vevő számára.
Szeretne időben értesülni az egészségügyi szektor újdonságairól? Iratkozzon fel hírlevelünkre most!
Tovább a hírlevél feliratkozáshoz
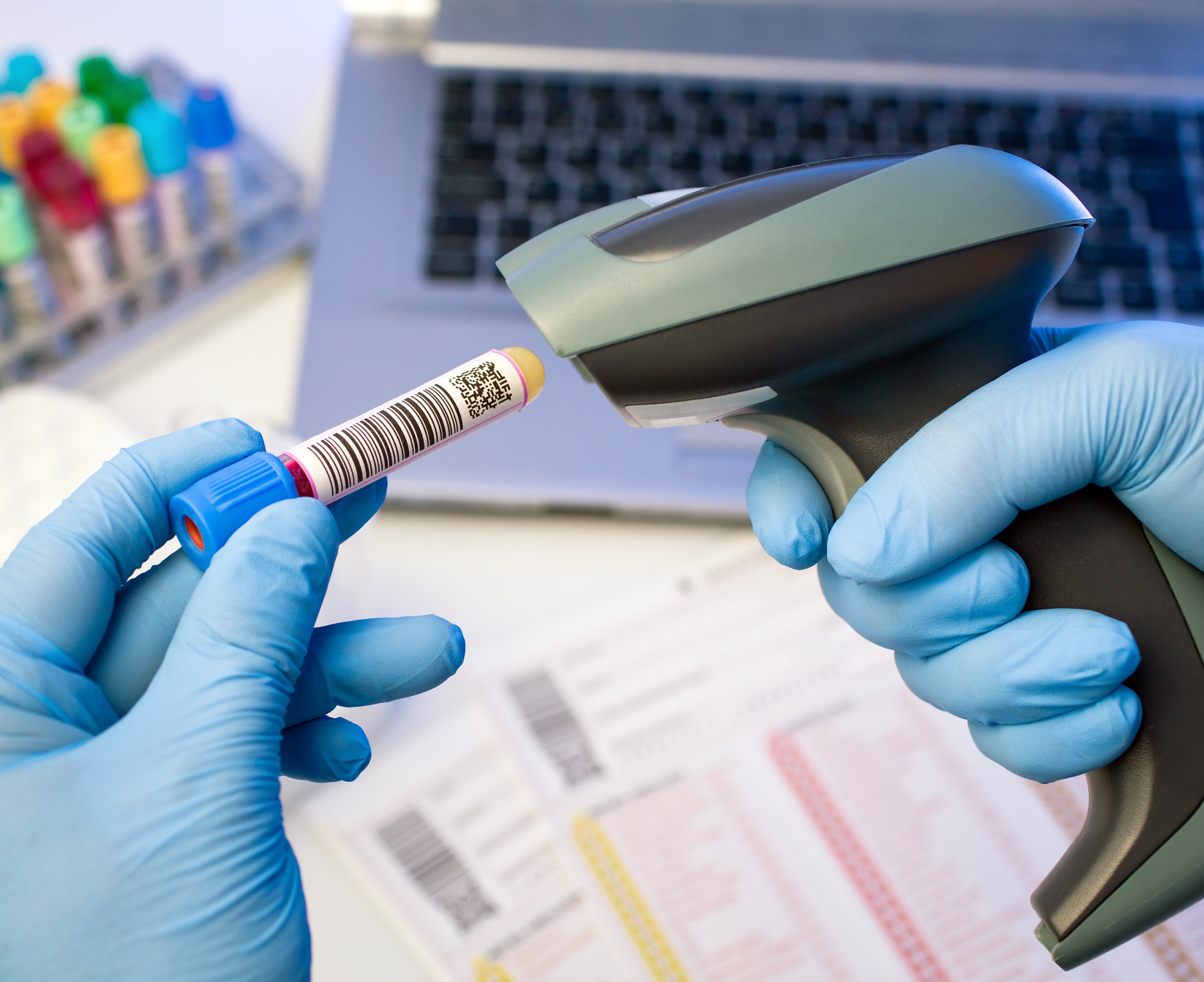 Az átmeneti időszakban, amikor a lineáris vonalkódok mellett megjelennek az új 2D-s kódok is a termékeken, fontos figyelembe venni, hogy ha a kódok túl közel vannak egymás mellett elhelyezve a csomagoláson, akkor nehézséget fog okozni a gyógyszertári kasszánál az, hogy a megfelelő kód kerüljön leolvasásra. Ezért a dokumentum szerint, amennyiben egydimenziós és kétdimenziós vonalkódok is elhelyezésre kerülnek a termékeken, ebben az esetben nem ajánlott a kódokat közvetlenül egymás mellett feltüntetni (2.3 kérdés).
Az átmeneti időszakban, amikor a lineáris vonalkódok mellett megjelennek az új 2D-s kódok is a termékeken, fontos figyelembe venni, hogy ha a kódok túl közel vannak egymás mellett elhelyezve a csomagoláson, akkor nehézséget fog okozni a gyógyszertári kasszánál az, hogy a megfelelő kód kerüljön leolvasásra. Ezért a dokumentum szerint, amennyiben egydimenziós és kétdimenziós vonalkódok is elhelyezésre kerülnek a termékeken, ebben az esetben nem ajánlott a kódokat közvetlenül egymás mellett feltüntetni (2.3 kérdés).
Készült kiegészítés arra vonatkozóan is, hogy engedélyezett ugyan a QR kód elhelyezése a termékeken, de azt csak marketing célból lehet feltüntetni, azonosítás és eredetiségellenőrzés céljából a DataMatrix kódot kell továbbra is használni. Felhívják a figyelmet arra is, hogy ha lehetőség van rá, akkor a QR kódba kódolt információt inkább a DataMatrixba kódolják, mivel adatkapacitás szempontjából ezt a DataMatrix kód is lehetővé teszi (azaz van benne elegendő hely erre a célra). Ha egy gyártó mégis mind a két kódot felhelyezné, akkor viszont a QR-t nem szabad a DataMatrix közvetlen közelébe tenni, annak érdekében, hogy elkerüljék a végfelhasználónál a téves kódbeolvasást. (2.12 kérdés).
Az EU Bizottság kimondta, hogy a kódban elhelyezett információknak pontosan meg kell egyezniük az adatbázisokba feltöltött adatokkal, és ezért elengedhetetlen, hogy a gyártó és a forgalombahozatali engedély tulajdonosa szorosan együttműködjön. (4.5 kérdés).
Annak tisztázására is készült kiegészítés, hogy az Európai Bizottságot hogyan kell tájékoztatni a hamisításokról (7.17 kérdés).
Az angol nyelvű dokumentum az alábbi linken érhető el: https://ec.europa.eu/health/sites/health/files/files/falsified_medicines/qa_safetyfeature_en.pdf
