Az Európai Unió sokat emlegetett két új rendelete (MDR 2017/745 és IVDR 2017/746) értelmében olyan szervezetek kerülnek kijelölésre, amelyek felhatalmazást kapnak a rendeletekben érintett orvostechnikai eszközök megfelelőségének értékelésére és amelyek erről tanúsítványt állíthatnak ki, szigorú kritériumok alapján. Mostanáig hivatalosan 9 szervezet kapott ilyen engedélyt és továbbiak kijelölése várható, köztük magyar szervezet elbírálása is folyamatban van.
 A bejelentett szervezetek kijelölésének folyamata még nem zárult le, 2020-ban még 3 szervezet kijelölése biztosan esedékes lesz, emellett a 2020-ra átcsúszott 4 helyszíni audit, 3 fennmaradó JAT (Joint Assessment Teams) elfogadás, illetve a hiányzó 8 végső jelentés függvényében további szervezetek kijelölésére is sor kerülhet. A kérelmet 2017. november 26-tól kezdődően adhatták be a pályázó szervezetek, akikre ezt követően egy közel 12 hónapos kijelölési eljárás vár, mind nemzeti, mind európai hatóságoknál működő értékelők bevonásával. Tudomásunk szerint a magyar szervezetek közül a CEcertiso Kft. már beadta a kérelmet és a helyszíni auditon túl van, továbbá az OGYÉI-EMKI is megkezdte a felkészülést az MDR kijelölés megkezdéséhez.
A bejelentett szervezetek kijelölésének folyamata még nem zárult le, 2020-ban még 3 szervezet kijelölése biztosan esedékes lesz, emellett a 2020-ra átcsúszott 4 helyszíni audit, 3 fennmaradó JAT (Joint Assessment Teams) elfogadás, illetve a hiányzó 8 végső jelentés függvényében további szervezetek kijelölésére is sor kerülhet. A kérelmet 2017. november 26-tól kezdődően adhatták be a pályázó szervezetek, akikre ezt követően egy közel 12 hónapos kijelölési eljárás vár, mind nemzeti, mind európai hatóságoknál működő értékelők bevonásával. Tudomásunk szerint a magyar szervezetek közül a CEcertiso Kft. már beadta a kérelmet és a helyszíni auditon túl van, továbbá az OGYÉI-EMKI is megkezdte a felkészülést az MDR kijelölés megkezdéséhez.
Az MDR és IVDR Rendeletek szerint az irányelvek alapján kiadott tanúsítvánnyal (MDD/AIMDD tanúsítvánnyal) rendelkező eszközök 2024. május 25-ig továbbra is forgalomba hozhatók és 2025. május 25-ig forgalmazhatók. Ez azt jelenti, hogy az MDD és AIMDD tanúsítványok lejáratáig a jelenlegi bejelentett szervezetek kötelesek az auditokat végrehajtani, továbbá a tanúsítványok fenntartását támogatni.
Az Európai Bizottság által a napokban publikált statisztikai áttekintés szerint 2017-től kezdődően az MDR és IVDR Rendeletek összefüggésében mintegy 55 szervezet adta be a bejelentett szervezetté váláshoz szükséges kérelmet, amiből 2019 végéig 9 szervezet került publikálásra.
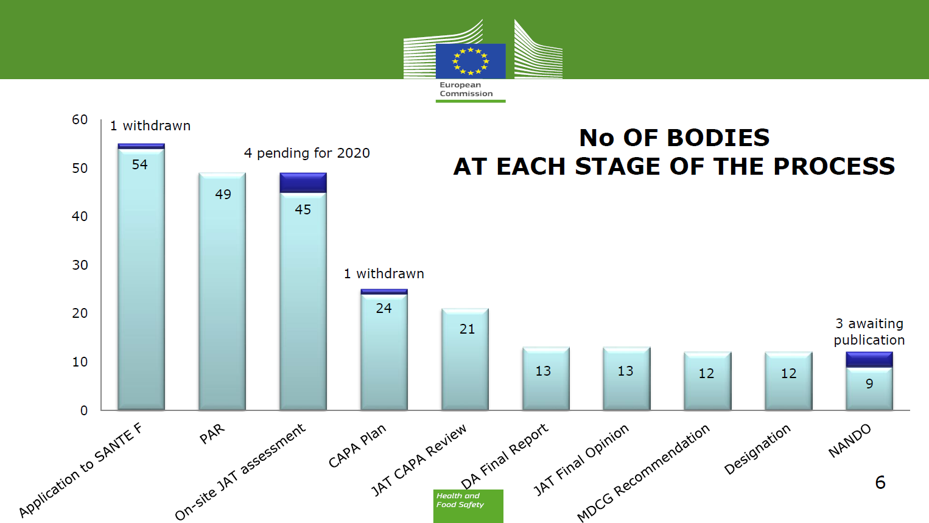
Az elemzés megerősíti, hogy összesen 44 MDR és 11 IVDR kérelem érkezett be, amelyből 49-et fogadott be az Európai Bizottság SANTE csoportja. Ez az MDD és AIMDD Irányelvek alapján kijelölt bejelentett szervezetek 74%-át jelenti. A 49 kérelem közül 45 esetben a helyszíni ellenőrzésre már sor került, a fennmaradó 4 esetben (2 MDR és 2 IVDR kérelem) pedig 2020-ban várható a helyszíni audit elvégzése. A helyszíni értékelést követően a kijelölő hatóság megköveteli a kérelmet benyújtó megfelelőségértékelő szervezetektől, hogy meghatározott határidőn belül készítsék el a javító és megelőző intézkedéseket tartalmazó ún. CAPA-tervet (Corrective and Preventive Action), amelyet eddig 25 kérelem esetében teljesítettek. Ebből a 25 CAPA-tervből 1 visszavonásra került, a fennmaradó 24 élő tervből a JAT értékelő csoportja 2019 végéig 21-et fogadott el (3 elfogadása még folyamatban van). A JAT által elfogadott CAPA-terv közül 13 esetben készült el a végső jelentés, amelyből az MDCG koordinációs csoport 12-őt el is fogadott, azonban 3 publikálása még várat magára 2020-ban.
Az MDCG által elfogadott és kijelölt bejelentett szervezetek a NANDO (New Approach Notified and Designated Organisations) adatbázisban kerülnek publikálásra, amely az alábbi oldalon keresztül, a megfelelő jogszabályra kattintva (Regulation (EU) 2017/745 on medical devices vagy Regulation (EU) 2017/746 on in vitro diagnostic medical devices) érhető el:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.main
A cikk írásának időpontjáig az alábbi bejelentett szervezeteket jelölték ki az MDR-hez:
- NB 0086 BSI Assurence UK Ltd - United Kingdom
- NB 2797 BSI Group The Netherlands B.V. - Netherlands
- NB 1912 DARE!! Services B.V. - Netherlands
- NB 0344 DEKRA Certification B.V. - Netherlands
- NB 0124 DEKRA Certification GmbH - Germany
- NB 0051 IMQ Istituto Italiano del Marchi di Qualitá S.P.A. - Italy
- NB 0482 MEDCERT ZERTIFIZIERUNGS- UND PRÜFUNGSGESELLSCHAFT FÜR DIE MEDIZIN GMBH - Germany
- NB 0197 TÜV Rheinland LGA Products GmbH - Germany
- NB 0123 TÜV SÜD Product Service GmbH Zertifizierstellen – Germany
A cikk írásának időpontjáig az alábbi bejelentett szervezeteket jelölték ki az IVDR-hez:
- NB 0086 BSI Assurence UK Ltd - United Kingdom
- NB 2797 BSI Group The Netherlands B.V. - Netherlands
- NB 0124 DEKRA Certification GmbH - Germany
Hasznos friss hírekért iratkozzon fel Egészségügyi hírlevelünkre még ma!
Tovább a hírlevél feliratkozáshoz
